循環器内科
心臓電気生理

異常に遅い脈(徐脈)と、異常に速い脈(頻脈)に分けられ、時には生命を脅かす危険な不整脈となる場合もあります。不整脈の検査や治療について、わかりやすくご説明します。
不整脈とは
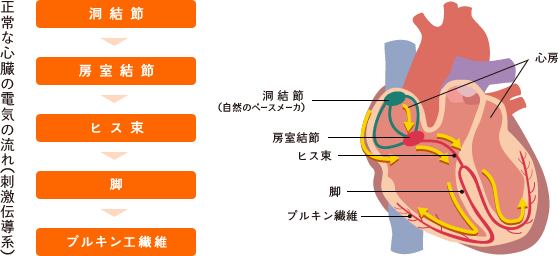
心臓の動くリズムは、刺激伝導系と呼ばれる特殊な心筋組織に電気が流れ、その電気的興奮が心筋全体に伝わって心臓が収縮と拡張を繰り返します。刺激伝導系の最も上流にある洞結節は、右心房と上大静脈の接合部に位置しており、ここから電気が流れることでまず心房が収縮し、ついで電気的興奮が心室に波及することで心室が収縮します。
洞結節は自律神経に支配されていて、安静時の心拍数は毎分60~100ですが、運動や緊張により自律神経が興奮すると、心拍数は徐々に上昇します。正常な心臓では自律神経と刺激伝導系の連携により、常に必要なだけの血液が全身に供給されるように心拍数が自動的に調節されているわけです。このような仕組みが破綻し、心臓がうまくリズミカルに動かなくなった状態を“不整脈”といい、不整脈と一言にいっても様々な種類の不整脈があります。
不整脈は大きく分けると異常に遅い脈(徐脈)と速い脈(頻脈)に分けられます。突然発生する異常な脈は動悸や胸の不快感の原因になるばかりか、めまいやふらつき・失神を来たします。時には生命を脅かす危険な不整脈となる場合もあります。
カテーテルアブレーション
- 不整脈と診断され、不安にかられていませんか?不整脈にも様々な種類があり、病状や治療法は人によって様々です。
- 代表的な不整脈である心房細動は、自覚症状が強くなければ、多くの場合は急ぎません!慌てて治療について決断する必要はないので、まずは病気を理解しましょう!
- 当院では、不安をかきたてることなく、外来でじっくり時間と回数をかけて専門医が分かりやすく説明することを大切におります。一緒に病気と向き合い、納得した上で、カテーテルアブレーション治療で根治を目指しましょう!

(診察室でのイラストを用いた病状説明の様子)
不整脈の中でも、心臓の動きが正常値を超えて速く動く状態を「頻脈性不整脈」と呼びます。カテーテルアブレーション(経皮的心筋焼灼術ともいいます)は、過剰な伝導路(心筋を動かす電気の通り道)や不整脈の焦点を、カテーテルを用いて焼いてしまう方法です。以下のような疾患に有効となります。
- 発作性又は持続性心房細動
- 心房粗動
- 心房頻拍
- 心室性頻拍症など、心室性不整脈
- WPW症候群に伴う房室回帰性頻拍
- 房室結節リエントリー性頻拍などの発作性上室性頻拍症
アブレーション治療では、カテーテルを主に足の付け根にある太い血管から入れ、心臓まで到達させます。カテーテルの先には局所心筋の電気信号を計測するための電極がついていて、それで心臓の内壁に接触させながら電気信号を計測します。この計測によって、今カテーテルが接している部分が、異常な部位であるかどうかがわかります。この異常な部分を探す作業のことを「マッピング」と呼びます。心臓の異常な部分を示す”地図(マップ)”をつくる作業です。
異常な部分があることがわかったら、次にカテーテルの先の電極から高周波電流を流します。強い電流によって、カテーテルの先に触れているわずかな領域の心臓組織だけが電気的に焼かれて、細胞は死滅します。1回の焼灼あたり、電流を流す時間は1分以内、焼灼範囲は直径、深さとも5mm程度です。
また、近年では、様々な治療のエネルギーが開発され、急速に発展して普及しているのが、冷凍エネルギーである「クライオアブレーション」です。
特に、治療症例の過半数を占める、心房細動に対する治療であるクライオバルーンが標準的治療として普及しております。肺静脈ごとに一括隔離することができ、シンプルな方法で治療時間の短縮にもつながります。日本不整脈学会心電図学会が定めている不整脈専門医研修施設に該当する当院では、本治療法も取り入れて施行しております。
日本国内において最先端治療をしている環境で修練を積んだ専門医が、患者様ごとに病型や治療対象となる肺静脈の形態に合わせて最適な治療手段を選択させて頂きます。
是非、当院外来にお越しいただき、得体の知れない不安を取り除くべく、病気に向き合って、最適な治療について納得いくまで考えていきましょう。治療の概要や方法、入院期間など具体的に説明をさせて頂きます。かかりつけ医からの診療情報があれば、是非ご提供下さい。特に発作性の不整脈は診断には、不整脈出現時の心電図が必須ですので、ご持参いただくと診断と治療までの流れがスムーズになります。
- 当科では医療費削減並びに地球環境の負荷軽減に取り組んでいます。このため再製造単回使用医療機器を治療にて使用する場合があります。(再製造単回使用医療機器の詳細についてはこちらを参照ください)
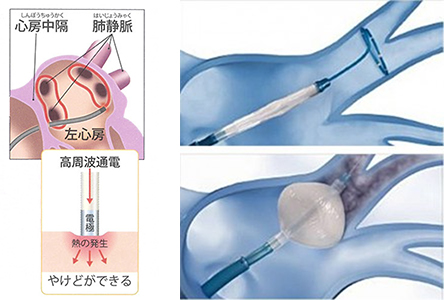
(心房細動に対するカテーテルアブレーション治療の模式図)
左図は、高周波カテーテルアブレーション治療。右図は冷凍エネルギーを用いたクライオバルーンアブレーションです。個々の病状に応じて適した治療方法を選択しております。
部門責任者:吉澤 尚志
心臓デバイス治療
- ペースメーカー・植込み型除細動器(ICD)・心臓再同期療法(CRT)
-
1950年代に洞不全症候群や房室ブロックといった徐脈性不整脈に対するペースメーカー療法は開発が始まりました。ペースメーカーは心臓にもともと備わった自然のペースメーカーの代わりを務める医療用電子機器です。心臓の鼓動が遅くなったことを検知すると、ペースメーカーは電気的刺激を心臓に送り、正常なリズムで鼓動させるようにします。我が国では1970年台より急速に普及し、1980年代には小型化、電池寿命の延長、生理的ペースメーカーの開発などペースメーカー治療は進歩してきました。
また、心室頻拍・心室細動など致命的な頻脈性不整脈に対する治療として1980年代に植込み型除細動器(ICD)が開発されるようになりました。植込み型除細動器は除細動器とペースメーカーの機能を併せ持っています。頻脈性不整脈を検知すると抗頻拍ペーシングや電気ショックを行い頻脈性不整脈を治療します。
さらに、心臓の機能が低下する心不全への治療として1990年代以降両室ペーシングによる心臓再同期療法(CRT)が確立され普及するようになりました。心臓再同期療法は前述のペースメーカーに加え、左室ペーシングの機能が追加されています。従来は右室ペーシングのみですが、さらに左室ペーシングを行い、心室の収縮のタイミングがずれる同期不全を改善させることで、心不全を治療します。
以上のように植込み型心臓デバイスによる治療は徐脈性不整脈から始まり適応疾患を拡大させながら発展・普及しており、当院では適応をしっかりと判断した上でこれらの心臓デバイス治療を行っております。ペースメーカーはジェネレーター本体と電気刺激を伝えるリードからなります(図1)。リードを心臓の内に挿入し固定をし、ジェネレーター本体と接続して、ジェネレーター本体を皮膚の下側に植込む手術です。ジェネレーター本体はリードを介して心臓の電気的興奮を監視し、設定された心拍数より少なくなる時に心臓に電気刺激を物理的に与え、心拍を確保し徐脈を改善させます。 手術では、まず肩の鎖骨の下側の皮膚を切開し皮下ポケットを作ります。そこから血管を穿刺、もしくは血管を剥離切開してカテーテルを挿入し、カテーテルを通してリードを心臓の要所に挿入し配置します。つぎに、リードから電気刺激を行い試験を行います。心臓の反応がよい位置が見つかるまで、これを繰り返します。良好な位置でリードが抜け移動しないよう固定し、リードをジェネレーター本体と接続します。最後にリードとジェネレーター本体を皮下ポケットにおさめて、皮膚を縫合します(図2)。手術の所要時間や成功率、危険性は不整脈の種類によって異なります。また、同じタイプの不整脈でも、人によって心臓の大きさや形が異なるため、難易度も異なってきます。ペースメーカー移植術の平均的な手術時間は約1~3時間です。 手術後は約1週間ほど入院で経過をみていきます。この間合併症の有無をチェックしていきます。術後の合併症は出血、感染、気胸、心タンポナーデ、リード移動などがありますが、致命的な合併症は非常にまれです。 退院後は基本的には普段通りの生活が送れます。ただし、ペースメーカーなど植込み型心臓デバイスは電磁波の影響を受けるため、電磁波への暴露を避ける必要があり、多少の注意が必要です。退院後は電池の残量やペースメーカーの作動状況などを調べるために概ね3~6か月ごとに、ペースメーカー外来を受診する必要があります。また最近では遠隔モニタリングといって、植込み型心臓デバイスは、電池の残量やリードの状態、不整脈の発生など様々な情報を自宅から病院にインターネットを介して送信できるようになっています。電池の寿命は機種や患者さんの状態によって十人十色で、4~10年程度と幅があります。電池が減ってくると本体の入れ換えが必要になります。一般的には交換術では本体だけが交換され、リードはそのまま使われますので、最初の植込み手術よりも短時間で終了します。

図1. ペースメーカージェネレーター本体とリード
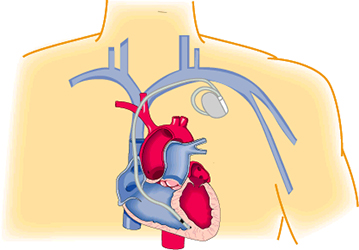
図2. ペースメーカー移植術
- リードレスペースメーカー
-
ペースメーカーには、今まで本体にリードと呼ばれる導線が付いているリード付きペースメーカーのタイプしかありませんでしたが、2017年9月、リードレスペースメーカーが登場しました。リードレスペースメーカーとは、洞不全症候群や房室ブロックで、徐脈を起こした患者さんの脈拍を正常に保つよう、補助的に電気信号を送るペースメーカーですが、リードが不要で本体は小さなカプセル型をしており、電気回路や電池、電極などの全てが組み込まれており、先端に付いているハネのような部分を心臓の内部に固定します (図3) 。

図3. リードレスペースメーカーリードレスペースメーカーは、本体を皮下に植え込むのではなく、足の血管からカテーテルを用いて心臓内にリードレスペースメーカー本体を送り込み、直接右心室に留置します。従来のペースメーカーと異なり、胸部の皮下ポケットもリードも不要なため、リードの断線、静脈閉塞、皮下ポケットからの感染などの合併症のリスクが少なくなり、手術による胸の傷や皮下に植え込まれた本体装置のふくらみがなくなります。(図4)
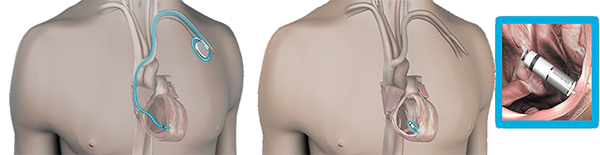
図4. 従来のペースメーカー(左)とリードレスペースメーカー(右)手術は約1時間と従来のペースメーカー植込みより短くなります。電池が消耗した場合従来のペースメーカーですと皮膚を再切開して本体のみを取り出して交換しますが、リードレスペースメーカーは心臓内にひっつくため取り出せず、2つめを再び挿入することになります。リードレスペースメーカーは現段階では右室のみの動作となるため、従来のペースメーカーのように右房と右室両方に働きかけられないため、すべての徐脈性不整脈の方に適応となるわけではありません。徐脈性心房細動や、短時間のみ徐脈の発作を起こす方などが良い適応と考えております。患者様の不整脈のタイプやご病状に応じて、従来のペースメーカーかリードレスペースメーカーのどちらが望ましいかよく検討して手術に臨んでいます。
- 皮下植込み型除細動器
-
植え込みデバイス(ICD)は心室頻拍や心室細動といった、瞬時に血圧低下を来し失神を起こしたり、突然死の原因となる頻拍性不整脈の医療機器です。従来のICDはペースメーカーと同じく、不整脈を診断・記録し、治療が必要なときに電気ショックを発生するICD 本体と血管内から心臓内に挿入され、心臓の心拍を本体に伝えたり、電気ショックの電流を心臓に与えるリードで構成されています(図5左)。リードを挿入する手術の際に稀ですが、肺や血管・心臓によってリードが傷つくことがあります。また、ICD本体やリードの感染やリード断線によってICD動作に不具合が生じた場合、リード抜去を行う必要があります。皮下植込み型除細動器(S-ICD)は新しい種類のICDで、従来のICDと同様に本体とリードで構成されていますが、リードは血管内から心臓内に挿入せず、皮下に植え込みます(図5右)。
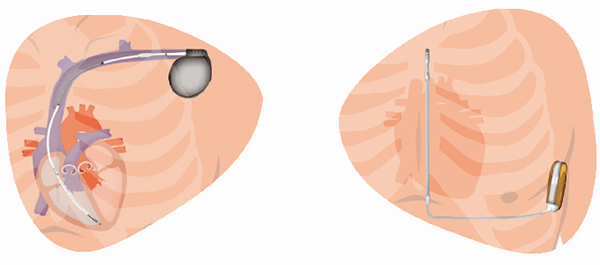
図5. 従来の経静脈ICD(左)と皮下植込み型除細動器(S-ICD) (右)S-ICDの手術は全身麻酔で行うことが多く、左胸のわきの皮下に本体を植込み、リードを胸骨の横に皮膚の下を通して植込みます(図6)。手術は約1~2時間ほどで終了します。従来のICDとS-ICDで治療の有効性に違いはありませんが、S-ICDは徐脈のときにペーシングや心室頻拍に対して抗頻拍ペーシングによる治療が行えないため、それらの治療が必要・有効と予想される場合は従来のICDの適応があると考えています。
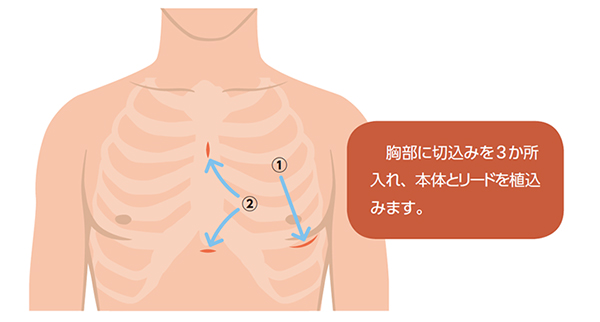
図6. S-ICDの手術 - 植込み型ループレコーダー
-
植込み型ループレコーダーは長さ約4cmほどの小ささですが、左胸の皮下に植込み約3年間にわたり、心電図を記録することのできる検査機器です。ホルター心電図など通常の診断方法では検出が難しい不整脈の発作が、発作が起こったときに記録することができます。突然意識を失って倒れることを失神といいますが、通常の検査では原因不明な場合に、植え込み型ループレコーダーを植込み、失神が起こったときの心電図を記録することで不整脈を発見するのに用います。
また、脳梗塞症を発症した方で、脳梗塞症のタイプが心臓から血栓がとんで脳の血管に詰まる心原性脳塞栓症が疑われる場合、その血栓の原因となる不整脈である心房細動を見つけるために植込むことがあります。
図7. 植え込み型ループレコーダー手術は局所麻酔で胸の皮膚を1 cmほど切開し、機器を胸の皮下に植え込みます。約10~30分ほどと短時間で終了します(図8)。脳梗塞症の原因を調べる際に植込む場合は、事前に脳神経内科・脳神経外科の医師と協議して、協力して植込み手術を行っています。植込み後は普段通りに生活が可能で、失神など症状があった時に専用の携帯型リモコンを操作していただき、そのときの心電図を約7分間記録することも出来ます。診断がつき必要がなくなった場合は体外に摘出します。
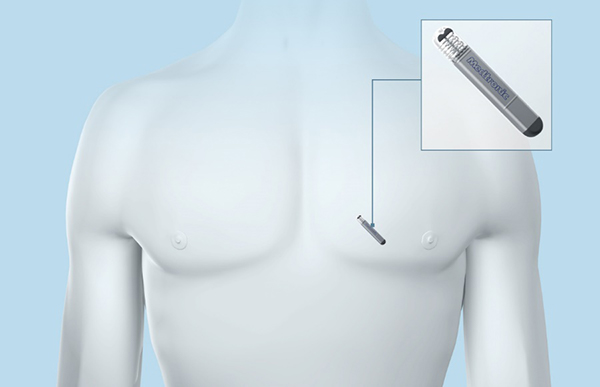
図8. 植え込み型ループレコーダーの手術
部門責任者:小川 尚


